PET検査用薬剤合成装置「FASTlab」および「FASTlab 2」で合成されるアミロイドPETイメージング剤「ビザミルTM」を用いた検査が保険適用へ
PR TIMES / 2024年10月2日 21時45分
~アルツハイマー型認知症診断へのさらなる貢献を目指す~
医療の課題解決に取り組むGEヘルスケア・ジャパン株式会社(本社:東京都日野市、代表取締役社長兼CEO:若林 正基)は、PET(陽電子放射断層撮影装置)検査で使用する放射性薬剤を自動合成する放射性医薬品合成設備「FASTlab(ファストラボ)」および「FASTlab 2(ファストラボツー)」で合成されるアミロイドPETイメージング剤「ビザミルT(TM)(VIZAMYL(TM)、一般名:フルテメタモル)、以下”ビザミル”」を用いた検査が、10月 1日付けで保険適用*されることとなりましたのでお知らせします。
[画像1: https://prcdn.freetls.fastly.net/release_image/51346/109/51346-109-ecf94dc95e0262cb9c678cf8bbef2668-1673x885.jpg?width=536&quality=85%2C75&format=jpeg&auto=webp&fit=bounds&bg-color=fff ]
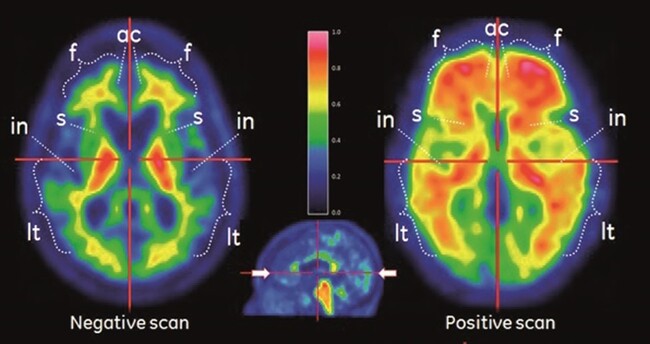
アミロイドβ 陰性画像(negative scan)と陽性画像(positive scan)
国内では昨年、アルツハイマー病による軽度認知障害および軽度の認知症の進行抑制を効能又は効果とする治療薬(疾患修飾薬)の販売が開始されましたが、この治療薬の処方判断の方法の一つとして承認を受けた診断法によりアミロイドβ病理を示唆する所見を確認することが求められています。ビザミルは、アルツハイマー病による軽度認知障害又は認知症が疑われる患者の脳内アミロイドβプラークを可視化するPET用薬剤です。このことから、ビザミルによるアミロイドPET検査は、非侵襲的に脳内のアミロイドβの沈着を評価できる検査方法として大きな期待と注目が寄せられ、アルツハイマー病の早期診断や適切な治療へ活用されています。
GEヘルスケア・ジャパンは、2015年5月に「FASTlab」でのビザミル合成機能について「アルツハイマー型認知症が疑われる認知機能障害を有する患者の脳内アミロイドベータプラークの可視化」を効能・効果として薬事承認を取得し、2023年10月にはアルツハイマー病による軽度認知障害が疑われる患者も対象とする承認を取得しました。
現在、国内でPET・PET/CT・PET/MR装置を保有されているご施設約400施設のうち、サイクロトロンを保有しPET放射性薬剤の院内合成を行っているご施設は約150施設あります**が、この度の「FASTlab」および「FASTlab 2」で合成したビザミルを用いた検査が保険適用*されることにより、PET放射性薬剤の院内合成を行う全国のより多くの医療機関でアミロイドPET検査が広がることが期待されます。
[画像2: https://prcdn.freetls.fastly.net/release_image/51346/109/51346-109-c0ee5f00a9fc0cae05dbe7ed3c3cf4c0-742x366.png?width=536&quality=85%2C75&format=jpeg&auto=webp&fit=bounds&bg-color=fff ]
放射性医薬品合成設備FASTlab2
「FASTlab」は、2015年に国内で初めて1台で複数のPET用薬剤(FDGおよびビザミル)が合成可能な装置として承認を取得しました。疾病診断にPET装置を活用しサイクロトロンによる院内合成を実施するご施設において、限られたスペースおよび時間内で1日に2剤の合成が可能であることは設備投資やワークフローの面で効率的で有用なインフラとなります。また、半減期を有する放射性医薬品には製薬会社からの供給(デリバリー)が難しい地域があるため、医療の均てん化という意味においても院内合成は重要な役割を果たすと考えています。
超高齢社会を迎えた日本では、2025年には国内の認知症患者数が700万人を超え、高齢者の約5人に1人が認知症になるとの推計がされています***。アルツハイマー病による軽度認知障害および軽度の認知症の進行抑制を効能効果とする治療薬の適正使用のために、今後もアミロイドPET検査が大きな役割を果たすことを期待しています。
*厚生労働省の定めるレカネマブ(遺伝子組換え)製剤に係る最適使用推進ガイドラインに沿って、アルツハイマー病による軽度認知障害又は軽度の認知症が疑われる患者等に対し、レカネマブ(遺伝子組換え)製剤の投与の要否を判断する目的でアミロイドβ病理を示唆する所見を確認する場合、及びレカネマブ(遺伝子組換え)製剤の投与中止後に初回投与から18か月を超えて再開する場合に適用
**日本核医学会PET核医学分科会 https://jcpet.jp/facilities/
***認知症施策推進総合戦略
(新オレンジプラン:https://www.mhlw.go.jp/file/06-Seisakujouhou-12300000-Roukenkyoku/nop1-2_3.pdf )
その他、本資料に記載された装置の製品名/薬事販売名/医療機器承認番号は以下の通り
[表: https://prtimes.jp/data/corp/51346/table/109_1_f024d400dc9c89dae37f2230cca00b9b.jpg ]
GEヘルスケア・ジャパンについて
GEヘルスケア・ジャパン株式会社は、GEヘルスケアの中核拠点の1つとして1982年に創設されました。予防から診断、治療、経過観察・予後管理までをカバーする「プレシジョン・ケア」の実現を目指し、インテリジェント機器やデータ分析、ソフトウェア、サービス等を提供しています。国内に研究・開発、製造から販売、サービス部門までを持ち、日本のお客様のニーズにお応えしつつ、日本が直面する医療課題の解決に取り組んでいます。日本における社員数は約1,500名、本社および60カ所の事業拠点があります。
詳細はホームページ https://www.gehealthcare.co.jp/ をご覧ください。
企業プレスリリース詳細へ
PR TIMESトップへ
この記事に関連するニュース
-
〈世界アルツハイマーデー〉新薬レカネマブが使用できる病院が増加、数年後にはさらなる光明も? それでも予防が一番大事…タバコ、お酒が好きな40、50代は要注意!
集英社オンライン / 2024年9月21日 10時0分
-
「最新!ボケない食習慣」認知症予防は食事から、WHOのお墨付き“地中海食”のススメ
週刊女性PRIME / 2024年9月14日 6時0分
-
PET用標識化合物合成装置「放射性医薬品合成設備 MPS200Aβ」の使用目的又は効果に関する一部変更承認取得のお知らせ
PR TIMES / 2024年9月13日 12時45分
-
アルツハイマー病を前駆期で検出し、認知機能低下を予測出来る新たな方法を開発
PR TIMES / 2024年9月10日 17時45分
-
90歳過ぎて友達は少なくなったけれど…新たな場所で新たな友を【第一人者が教える 認知症のすべて】
日刊ゲンダイDIGITAL / 2024年9月10日 9時26分
ランキング
-
1神田前財務官「日本はもはや大国ではない」「貢献する意志と能力があるのかに尽きる」…ADB総裁候補として意気込み
読売新聞 / 2024年10月6日 13時0分
-
2【BIC SIM】店頭申し込みでSIMフリーiPhoneを15,000円割引するキャンペーンを実施
PR TIMES / 2024年10月4日 21時40分
-
3鳥貴族、「値上げ」でも客数激増、次は海外に攻勢 大倉社長が宣言、「焼き鳥を世界言語にする!」
東洋経済オンライン / 2024年10月6日 8時0分
-
4家に使っていない「ビニール傘」が10本あります…。買いすぎを防ぐよい方法はないのでしょうか?
ファイナンシャルフィールド / 2024年10月6日 2時0分
-
5人里離れた絶壁にあえて出店 130席の“ぽつんと”レストランなぜ人気? 驚きの「バッドロケーション戦略」に迫る
ITmedia ビジネスオンライン / 2024年10月5日 6時15分
記事ミッション中・・・
記事にリアクションする
![]()
記事ミッション中・・・
記事にリアクションする

エラーが発生しました
ページを再読み込みして
ください










