造血幹細胞の発生初期を司るシグナル分子を解明
PR TIMES / 2024年11月19日 14時15分
[画像: https://prcdn.freetls.fastly.net/release_image/124365/181/124365-181-78a9f783c342901d7251e3560413b8ad-540x304.jpg?width=536&quality=85%2C75&format=jpeg&auto=webp&fit=bounds&bg-color=fff ]
【ポイント】
造血幹細胞*1は、胎児期に造血性内皮細胞*2から発生します。今回、この発生過程の初期段階を司るシグナル分子*3の一つを解明しました。
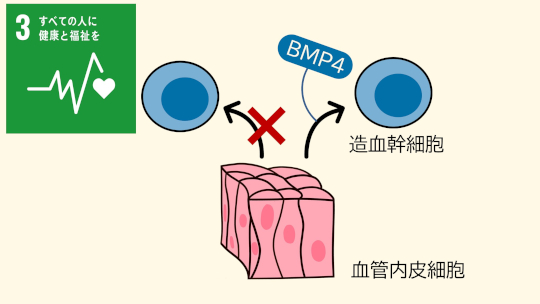
初期の造血性内皮細胞はBMP4*4の受容体を細胞表面に持っており、この細胞にBMP4を作用させることで、試験管内で造血幹細胞に分化させることに成功しました。
この研究成果は、ES細胞やiPS細胞などの多能性幹細胞*5から造血幹細胞を分化誘導するための培養法の確立に繋がることが期待されます。
【概要説明】
造血幹細胞は成体では骨髄に存在しますが、その起源は胎児期の大動脈内皮に遡ります。胎児の大動脈内皮に存在する造血性内皮細胞が造血幹細胞に分化します。造血性内皮細胞には初期と後期の異なる分化段階があり、後期の造血性内皮細胞から造血幹細胞への分化を調節するシグナル分子については解明が進んでいます。しかし、初期の造血性内皮細胞の分化を調節するシグナル分子は未だよく分かっていません。
今回、熊本大学発生医学研究所組織幹細胞分野の小川峰太郎教授、古賀沙緒里助教および鶴田真理子大学院生らの研究グループは、初期の造血性内皮細胞が造血幹細胞に分化するために必要なシグナル分子の一つがBMP4であることを明らかにしました。これまで本研究グループは、後期の造血性内皮細胞から造血幹細胞を分化させる培養系を作成しており、BMP4をこの培養系に応用することで、初期の造血性内皮細胞から造血幹細胞への発生過程を試験管内で再現することに成功しました。本研究成果は、将来的にES細胞やiPS細胞などの多能性幹細胞から造血幹細胞を作成する培養法の確立に繋がることが期待されます。
本研究成果は、国際幹細胞学会の機関誌「Stem Cell Reports」のオンライン版に2024年11月15日(日本時間)に掲載されました。本研究は、文部科学省科学研究費助成事業、公益財団法人日本科学協会笹川科学研究助成、熊本大学健康・生命科学S-HIGOプロフェッショナルフェローシッププログラム、公益財団法人肥後医育振興会医学研究助成金、熊本大学発生医学研究所共同研究拠点、熊本大学発生医学研究所高深度オミクス医学研究拠点ネットワーク形成事業、文部科学省共同利用・共同研究システム形成事業「学際領域展開ハブ形成プログラム」などの支援を受けて実施されました。
【展開】
ES細胞やiPS細胞などの多能性幹細胞から造血幹細胞を分化誘導するためには、胎児期における造血幹細胞の発生メカニズムの理解が必要です。本研究は、初期の造血性内皮細胞が必要とするシグナル分子の一部を明らかにしました。今後、造血幹細胞発生の初期段階を制御するシグナル分子の全容を解明することで、多能性幹細胞から造血幹細胞への分化誘導の実現に繋がるものと期待されます。
【用語解説】
1. 造血幹細胞:全ての血液細胞に分化できる能力と自分自身を複製する能力を併せ持つ幹細胞。胎児期に大動脈の内皮から発生し、成体では骨髄に存在する。
2. 造血性内皮細胞:血管を裏打ちする血管内皮を構成する血管内皮細胞のうち、血液細胞に分化する能力(造血性)を持つ特殊な細胞を造血性内皮細胞という。胎児期の大動脈に一時的に発生し、造血幹細胞の元になる。造血性内皮細胞には初期と後期の異なる分化段階がある。
*3. シグナル分子:細胞の機能を調節する信号を細胞に伝える分子。それぞれのシグナル分子に特異的な受容体を細胞が持ち、受容体にシグナル分子が結合すると、増殖、分化、遊走、活性化、不活化などの様々な細胞応答を引き起こす。タンパク質、脂質等、様々な物質がシグナル分子として働くことが知られている。
*4. BMP4:骨形成タンパク質(Bone morphogenetic protein)の一つ。骨など様々な組織の形成や、体の構造の形成など、幅広い役割を担うシグナル分子。
*5. 多能性幹細胞:胚性幹細胞(ES細胞)やiPS細胞など、個体を構成するすべての種類の細胞に分化することができる能力と自分自身を複製する能力を併せ持つ幹細胞。
【論文情報】
論文名:Bone morphogenetic protein 4 induces hematopoietic stem cell development from murine hemogenic endothelial cells in culture.
著者:Tsuruda, M., Morino-Koga, S., Zhao, X., Usuki, S., Yasunaga, K-i., Yokomizo, T., Nishinakamura, R., Suda, T., and Ogawa, M.(責任著者)
掲載誌:Stem Cell Reports
doi:10.1016/j.stemcr.2024.10.005
URL:https://doi.org/10.1016/j.stemcr.2024.10.005
▼プレスリリース全文はこちら
https://www.kumamoto-u.ac.jp/whatsnew/seimei-sentankenkyu/20241119
企業プレスリリース詳細へ
PR TIMESトップへ
この記事に関連するニュース
-
金属酵素の活性制御を応用して人工細胞の運命制御に成功
共同通信PRワイヤー / 2024年12月24日 10時0分
-
iPS受精卵作製研究容認へ議論 政府の生命倫理専門調査会
共同通信 / 2024年12月16日 17時54分
-
ヒトiPS細胞間での染色体導入を実現~ヒトiPS細胞を用いた疾患機序解明や再生医療研究への応用を期待
Digital PR Platform / 2024年12月6日 14時5分
-
血管をターゲットに! TGF-β/CD44抑制でがん血行性転移を阻止~がん転移の予防・治療への応用に期待
Digital PR Platform / 2024年12月5日 14時5分
-
長寿研究のいまを知る(12)細胞のリプログラミングはどこまで進んでいるのか
日刊ゲンダイDIGITAL / 2024年12月5日 9時26分
ランキング
記事ミッション中・・・
記事にリアクションする
![]()
記事ミッション中・・・
記事にリアクションする

エラーが発生しました
ページを再読み込みして
ください











